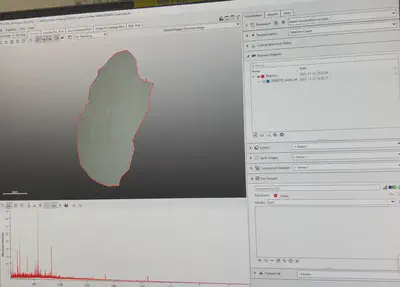
MALDI Imaging
 rapifleX
rapifleXMALDI开始前工作
在样品ITO玻璃板上未喷基质处点标准品(1 ul 多肽标准品和1 ul HCCA matrix混合),通风橱晾干后会自然结晶。用于调教系统及方法。
找到校正方法文件并复制到自己的实验文件夹
每次实验不改原始方法文件,复制到自己文件夹再进行修改。选择D/Methods/flexControlMethods/RP_600-3200_Da.par, 复制到自己的新建实验文件夹。
切换到上述方法
- 打开flexControl软件,然后file——select Method,选择方法par文件,一般采集方法需要和相应的标准品相匹配。
- 等待有下角的状态由黄变为绿,说明方法载入成功。

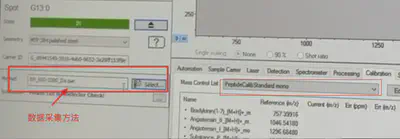
校正仪器,确保测量精度
选择Calibration——Peptidecalibstandard mono(适合m/z 700-4000之间),然后标准品会出现在Ref.Mass/Da列里面。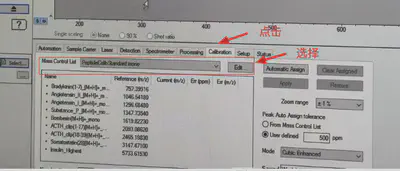
采集标准品的质谱图
- 视野中找到Standard样品,点状白色的结晶就是标准品和matrix的混合物。
- 十字中心点调至白色样品处,点击
Start开始开始采集标准品质谱图。瞬间旁边会出现质谱图。
- 点击
Automatic assign,自动对齐标准品和list理论值的峰图,只要Err在正负10之间就说明仪器正常。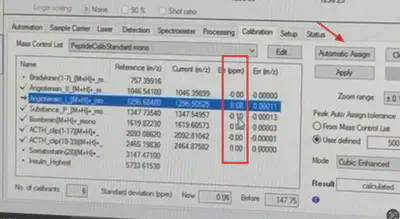
保存校正后的方法
- 点击
Apply - File——Save method
然后选择图像采集方法
- 复制图像采集方法
Imaging_Lipid_20µm.par到自己文件夹 - 载入该图像采集方法
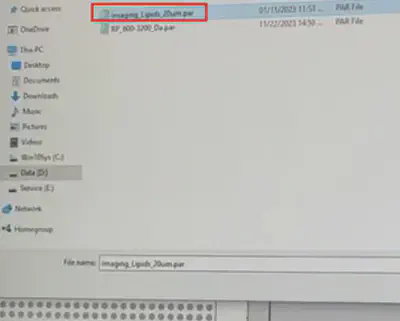
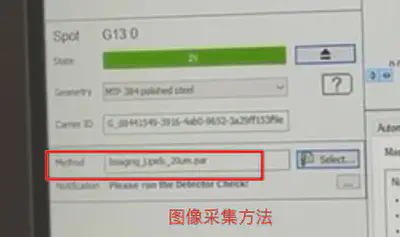
- 找到样品,先采集一针,根据丰度,可以调整激光强度。10^5左右的intensity就差不多。
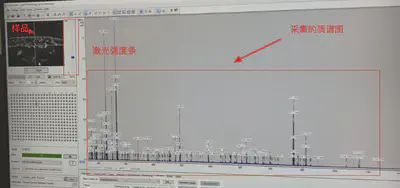
- 然后保存方法。
设置采集分辨率
- 一般根据你的需要进行调整,分辨率越高,采集时间越久。也就是两次激光距离越短,激光次数越多。
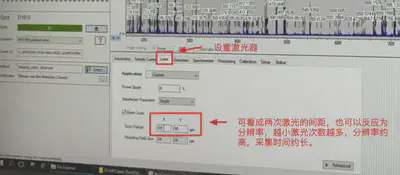
- 再次保存方法。
打开图像采集软件——fleximaging
打开软件,按右边的步骤一步步进行下去
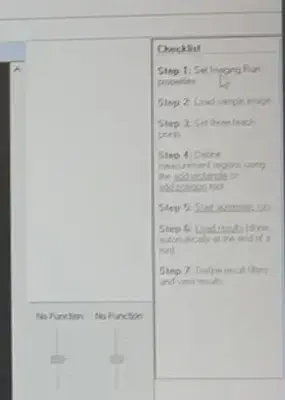
选择new imaging run,点击ok
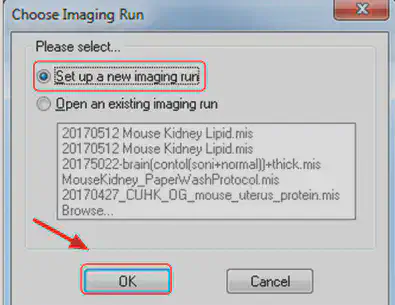
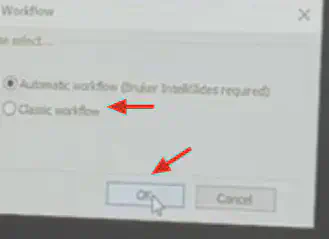
需要选择classic workflow,否则后面无法载入epson扫描文件。
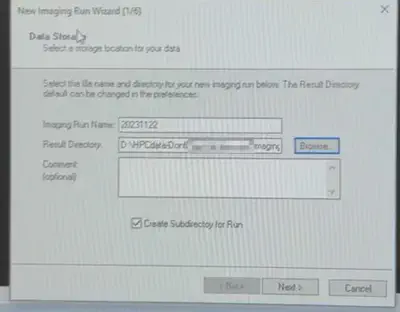
命名和选择结果保存文件夹
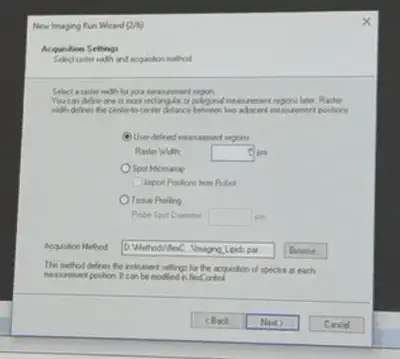
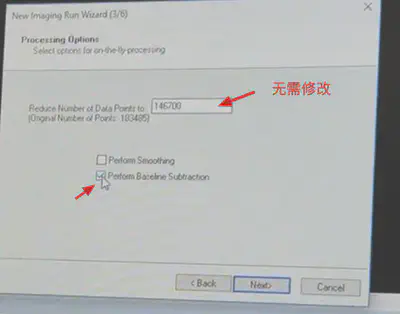
设置分辨率,和优化过的方法文件
选择baseline
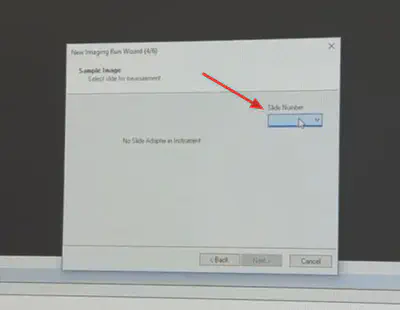
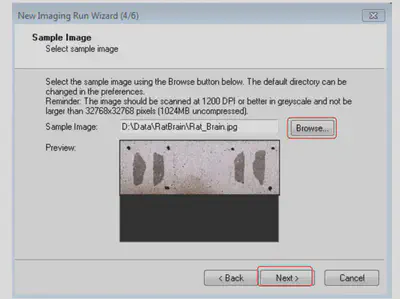
将之前扫描的样品位置照片放置此次实验文件夹下面,这样才能在这一步识别。否则不会出现。
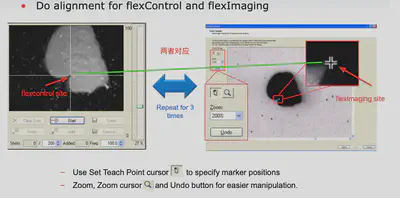
需要对齐flexControl和flexImaging,使得两边的位置一致,这样才能采集到正确的图。一般需要对应3-4个点。


用矩形工具或者无规则工具将需要采集的样品框起来。需要采集几个就框几个。

然后开始run,点击确定就可以,此时可能会卡顿,耐心等待。
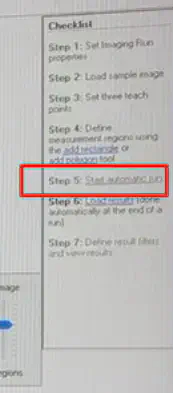
可以看到采集所需要的时间。分辨率高,且样品数多,就会需要几个小时,甚至几天的时间。
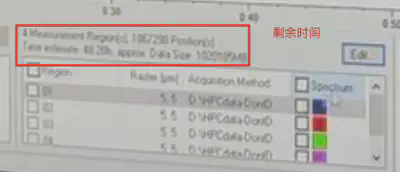
可以停止,进行调整,然后再次run
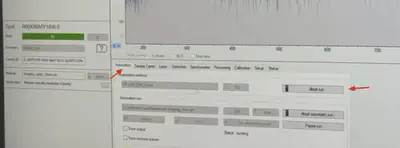
数据分析
使用SCiLS Lab软件进行数据分析,首先打开软件。
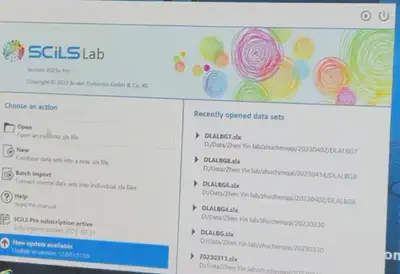
选择new,然后选择TOF,然后next

添加flexImaging采集的
.mis数据文件。
数据转换
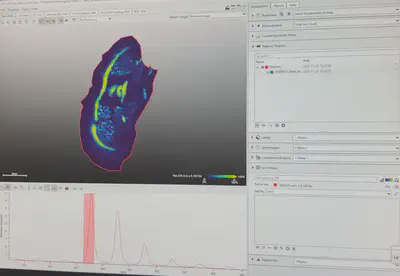
Next后,会出现总的图谱

然后
Import,选择文件夹存放,然后开始走进度条。

- 进度条结束后,就会出现这样的界面。可以选择你感兴趣的m/z。